| [ начало ] | [ К ] |
Камфарная кислота
— С 10 Н 16 О 4 = (СН 3)3 С 5 Н 5 (СО 2 Н) 2. Камфара при нагревании с металлическим натрием и ксилолом в продолжение суток до 280° и последующей обработке водой присоединяет элементы воды с разрывом одного из двух пятичленных колец и образованием таким образом камфоловой кислоты CH 3—C8H14—CO2 H. Кислота эта при окислении азотной кисл. дает двуосновную К. кисл.:
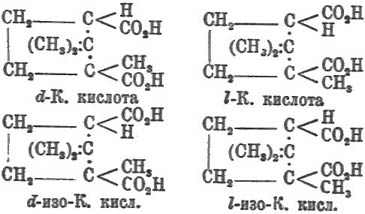
CO2H—C8H14—CO2 H. Можно К. кислоту получить и прямо из камфары продолжительным нагреванием этой последней с азотной кислотой. Впервые К. кислота получена была Козегартеном, а двуосновность ее была установлена работами Малагути, Либиха и Лорана. К. кислота известна в 4 оптически-изомерных формах, существование которых прекрасно объясняется бредовской формулой камфары. Схематически эти четыре конфигурации могут быть представлены так:
d- К. кислота получается окислением обыкн. камфары, а l- К. кисл. — окислением l- камфары. Темп. плавл. обеих модификаций 187°; (α)D (в спирт. раств.) = + 47,8°. l- Изокамфарная кислота получается из d- К. кислоты нагреванием ее в запаянной трубке с уксусной и соляной кислотами при 180°, а d- изокамфарная кислота тем же способом из l- К. Темп. пл. обеих изокамфарных кислот 171°; (α)D (в спирт. растворе) = —48°. Смесь растворов равных вес. частей d- и l- К. кислот дает рацемическую (r) форму К. кислоты, плавящуюся при 208°. r- Изокамфарная кисл. с темп. пл. 191° получается смешением кислот d- и l- изокамфарных или нагреванием с уксусной и соляной кисл. r- К. кислоты. К. кислоты легко при нагервании выше темп. плавления дают ангидрид, а изокамфарные ангидрида ни в этих условиях, ни при нагревании с хлористым ацетилом не образуют, что показывает, что карбоксилы в них находятся в trans-положении. Из всех К. кислот хорошо изучена только легкодоступная d-, или обыкн., К. кислота. При окислении перманганатом К. кисл. дает щавелевую и двуосновную кисл. состава C 8H12O5, при восстановлении HJ-м переходящую в αββ - триметилглутаровую. При окислении азотной кисл. конечным продуктом является камфароновая кислота С 9 Н 14 О 6 (см. соотв. статью). При действии сильных реагентов и высокой температуры К. кислота переходит в диметилциклогександикарбоновую кислоту, меняя пятичленное кольцо на шестичленное.
К. Дебу.
|
Page was updated:Tuesday, 11-Sep-2012 18:15:28 MSK |