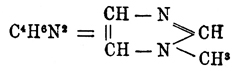 (Wallach).
(Wallach).| [ начало ] | [ О ] |
Оксамид
C2O2(NH2)2
— амид щавелевой кислоты. Впервые
получен Дюма (1830) при нагревании щавелево-аммиачной соли: С 2O4 (NН 4)2
= С 2O2 (NН 2)2
+ 2Н 2 O;
обыкновенно получается общей реакцией образования кислотных амидов, а именно
действием аммиака на сложные эфиры, в данном случае на щавелево-этиловый эфир: C 2O2(OC2H5)2
+ 2NH3 = C2O2(NH2)2
+ 2C2H5 (OH).
Образуется также гидратацией соответствующего нитрила, циана (см.): C 2N2
+ 2H2O = C2O2(NH2)2
(Liebig) при окислении синеродистых соединений, например желтой соли азотной
кислотой (Playfair), синильной кислоты перекисью водорода (Attfield) и т. п. О.
представляет белый, рыхлый кристаллический порошок, почти вовсе нерастворимый ни
в воде, ни в спирте, ни в эфире; при нагревании до 180° частью сублимируется, не
плавясь, частью разлагается на воду и циан; едкими щелочами в водном растворе
при нагревании гидратируется, превращаясь нацело в аммиак и щавелевую кислоту (в
ее соли); водный аммиак также гидратирует его при кипячении, но не вполне,
образуя оксаминовоаммиачную соль: C 2O2(NH2)2
+ H2O = C2O2(NH2)(NH4 O).
Из замещенных О. C 2O2N2H4-nRn
, где R = СН 3,
C2H5, C6H5
и т. п. и n = 1, 2, 3
и 4, известно много представителей. Они получаются обыкновенно действием
первичных и вторичных аминов на щавелевые, оксаминовые (см.) и замещенные
оксаминовые эфиры, а также дегидратацией щавелевых солей соответствующих аминов
при нагревании; представляют многочисленные случаи изомерии, большей частью
кристалличны, способны плавиться, сублимироваться и значительно более
растворимые чем О. При действии пятихлористого фосфора на симметрически
замещенные О. получаются хлоропродукты (например из С 2O2 (NН.CН 3)2
получается C 2Cl4(NH.CH3)2),
которые, легко теряя 3 частицы хлористого водорода, превращаются в содержащие
хлор основания, "хлороксалины", например C 4H5ClN2,
при восстановлении йодистым водородом, через замену Cl на H, дающие глюксалины,
например метилглиоксалин
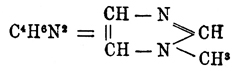 (Wallach).
(Wallach).
П. П. Рубцов. Δ .
|
Page was updated:Tuesday, 11-Sep-2012 18:16:02 MSK |