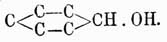
| [ начало ] | [ Т ] |
Тропин
С 7 Н 11 N(СН 3)(ОН) — главная составная часть алкалоидов, извлекаемых из многих пасленовых растений (Solanaceae). Название свое Т. получил от атропина, из которого он впервые и был получен Краутом. Алкалоиды вышеуказанных растений, атропин, гиосциамин, белладонин, гиосцин, скополамин, апоатропин и др., при кипячении с разведенными щелочами или баритовой водой распадаются все на кислоту и Т. или вещество весьма близко стоящее к нему. По исследованиям Ладенбурга, этот распад объясняется тем, что указанные алкалоиды представляют сложные эфиры карбоновых кислот и большею частью Т., поэтому он все их соединил в один класс, назвав тропеинами . Впоследствии им же были получены и искусственно многие тропеины этерификацией тропина более простыми ароматическими карбоновыми кислотами, и из них фенилгликоль-тропеин (Т. + миндальная кисл.) получил применение в медицине под названием гоматропина. Свободный Т. получается разложением атропина или гиосциамина баритовой водой или соляной кислотой:
С 17H23 NО 3 (атропин) + H 2 О = C 8 Η 15 ΟΝ (тропин) + С 8 Н 9 O.СО 2 Н (троповая кисл.).
При употреблении баритовой воды для разложения атропина, по удалении барита угольной кислотой в растворе остается троповокислый Т., который разлагается соляной кисл., и кислый раствор выщелачивается эфиром для удаления троповой кисл. Очищенный таким образом раствор хлористоводородной соли Т. концентрируется, соль разлагается окисью серебра, раствор, по обработке сероводородом для удаления следов серебра, выпаривается досуха, и остаток кристаллизуется из абсолютного эфира. Полученный таким образом Т. представляет бесцветные таблицы, плавящиеся при 61,2° — 63°. Т. кипит без разложения при 22 9 ° — 233°. Он весьма гигроскопичен и, легко растворяясь в воде и спирте, при испарения растворов выделяется в виде масла. Т. есть третичное однокислотное основание, дающее хорошо кристаллизующиеся двойные соли с хлорным золотом и хлорной платиной. Благодаря работам Ладенбурга и Мерлинга, строение Т. теперь можно считать окончательно установленным. Из работ Ладенбурга можно вывести следующие заключения. Так как Т. при сухой перегонке с натристой известью или гидратом окиси бария выделяет значительные количества метиламина СН 3 NН 2, то, вероятно, в нем имеется она метильная группа, связанная с азотом (= N.CH 3). Далее, так как Т. при осторожном окислении марганцовокалиевой солью не дает оксипродуктов, а переходит в тропигенин
С 7H12 О(NСН 3) + H2O = C7H13ON + CH3OH,
то, следовательно, он не имеет и двойных связей между углеродными атомами. При окислении же Т. хромовой кислотой в уксуснокислом растворе получается кетон тропинон:
C7H11(NCH3)OH + O = C7H10(NCH3)O + H2O,
указывающий, что гидроксил Т. связан не с первичными или третичным углеродам, а со вторичным. Окисляя же далее тропинон раствором хромовой кислоты в присутствии серной, Ладенбург получил тропиновую кисл. C 7H8(NCH3)(CO2H)2, которая была им переведена в нормальную адипиновую кислоту СО 2 Н.СН 2 СН 2 СН 2 СН 2.СО 2 Н. Этот факт указывает, что в Т. имеется углеродный скелет из 6-ти атомов, как в адипиновой кислоте; но так как эта последняя получается из нормального продукта окисления кетона, то вполне естественно предположить, что тропинон имеет в своем составе шестиатомное углеродное кольцо, которое, при дальнейшем окислении, разрывается у карбонильной группы, давая тропиновую кислоту; отсюда же непосредственно вытекает, что Т. имеет кольцо
Такой вывод подтверждается еще следующим фактом: Т. при кипячении с уксусной или соляной кислотой отщепляет воду и переходит в непредельное соединение тропидин: C7H10(NCH3), которое при действии марганцо-калиевой соли дает нормальный продукт окисления дигидрокситропидин C7H10(NCH3)(ОН) 2, переходящий при дальнейшем окислении в тропиновую же кислоту. Эти два ряда продуктов с достаточной вероятностью доказывали присутствие вышеуказанного кольца в строении Т., и Ладенбургу оставалось определить только положение еще одного атома углерода и группы NCH 3. Этого он достиг следующим образом. Тропидин при восстановлении цинком и соляной кислотой присоединяет, конечно, по месту двойной связи, два атома водорода и дает гидротропидин C7H12(NCH3), хлористоводородная соль которого при перегонке в струе хлористого водорода распадается на хлористый метил и норгидратропидин:
С 7H12 N(СН 3) + НСl = C 7H12 NH + СН 3Cl,
а этот последний при перегонке с цинковой пылью переходит в α-этилпиридин
На основании этих данных Т. должен иметь кольцо α-этилпиридина. Такие два вывода возможно совместить, только предположив существование в Т. сложного кольца из семи атомов углерода и одного атома азота, т. е. придав следующую формулу строения Т.
которая с достаточной простотой объясняет все указанные выше переходы. Если Ладенбург и доказал непосредственно существование в Т. пиридинового скелета, однако, для подтверждения выведенной им формулы строения Т. оставалось непосредственно же доказать существование гексаметиленового кольца, что и было выполнено Мерлингом, который рядом сравнительно простых переходов получил из Т. бромтолуол C 6H5.CH2 Br. Таким образом, после работ вышепоименованных ученых формула строения Т. была установлена, и только несколько неопределенным оставалось положение гидроксила, который мог находиться при том или другом углеродном атоме внутренней цепи. Однако, и этот вопрос был удачно разрешен Эйнгорном, определившим строение экгонина, который, являясь Т.-карбоновой кислотой, несомненно, должен иметь гидроксил там, где он написан в вышеприведенной формуле строения Т.
Д. Хардин, Δ.
|
Page was updated:Tuesday, 11-Sep-2012 18:16:43 MSK |